本實驗
K2S2O8(aq) 與
K2SO4(aq) 之濃度及離子電荷均相同,NaI(aq)
與
NaCl(aq)
之濃度及離子電荷均相同,如此當減少反應物取量體積時(如
K2S2O8(aq) 加
2 mL,則以
K2SO4(aq)補其體積),溶液中總離子電荷維持相等,
本年度曾經請助教試做實驗,以水代替
K2SO4(aq) 及
NaCl(aq)
補足反應液體積到
10 mL,發現反應物濃度雖相同,但速率較慢,即總溶液中離子數、
離子強度及計算公式,分析化學(Analytical
chemistry)課本有詳述,可到圖書館借閱,也請參考普化
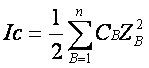 (CB
:molar
concentration of ion B;ZB
:charge
number of that ion)
(CB
:molar
concentration of ion B;ZB
:charge
number of that ion)